
셀트리온이 29일(현지시간) 미국 식품의약국(FDA)에 안과질환 치료제 ‘아일리아(성분명 애플리버셉트)’ 바이오시밀러 ‘CT-P42’의 품목허가를 신청했다고 30일 밝혔다.
셀트리온은 CT-P42의 글로벌 임상 3상 결과를 바탕으로 습성 황반변성(wAMD), 당뇨병성 황반부종(DME) 등 소아 적응증을 제외한 아일리아가 미국에서 보유한 전체 적응증에 대해 품목허가를 신청했다. 미국에 이어 유럽 등 글로벌 주요 국가에서도 순차적으로 CT-P42의 허가를 신청한다는 계획이다.
셀트리온은 체코, 헝가리, 폴란드, 스페인 등 총 13개국에서 당뇨병성 황반부종 환자 348명을 대상으로 진행된 임상 3상에서 오리지널 의약품 대비 동등성 및 유사성을 확인한 바 있다.
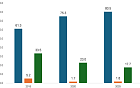
미국 리제네론(Regeneron)이 개발한 아일리아는 지난해 글로벌 매출 97억5699만 달러(약 12조6841억 원)를 달성한 블록버스터 안과질환 치료제다. 아일리아의 미국 독점권은 2024년 5월, 유럽 물질특허는 2025년 11월 만료된다.
셀트리온 관계자는 “미국을 시작으로 유럽 등의 주요 국가에도 허가를 순차적으로 신청하고 안과질환 영역으로 바이오시밀러 포트폴리오를 확장하는 데 최선을 다하겠다”고 말했다.
한편, 셀트리온은 CT-P42를 포함한 연내 최대 5개의 바이오시밀러의 글로벌 허가 신청을 완료한다는 계획이다.

![코스피 6000→7000까지 70일⋯‘칠천피’ 이끈 5대 고수익 섹터는?[7000피 시대 개장]](https://img.etoday.co.kr/crop/140/88/2330299.jpg)

![기본법은 안갯속, 사업은 제자리…인프라 업계 덮친 입법 공백 [가상자산 입법 공백의 비용①]](https://img.etoday.co.kr/crop/140/88/2329953.jpg)
![메가시티·해양·AI수도 3대 전장서 격돌…영남 민심은 어디로 [6·3 경제 공약 해부⑤]](https://img.etoday.co.kr/crop/140/88/2330190.jpg)
![BTL특별펀드, 첫 투자처 내달 확정…대구 달서천 하수관거 유력 [문열린 BTL투자]](https://img.etoday.co.kr/crop/140/88/2330175.jpg)
![[단독] “세종은 문턱 낮고, 서울·경기는 선별”…지역별 지원 ‘천차만별’ [붙잡은 미래, 냉동난자 中]](https://img.etoday.co.kr/crop/140/88/2330168.jpg)
















![“리튬 가치 아직 주가에 없다”...포스코홀딩스 재평가 시작되나 [찐코노미]](https://img.etoday.co.kr/crop/300/170/2330474.jpg)
![세리머니 코스피, 7384.56 마감…6.45% '급등' [포토]](https://img.etoday.co.kr/crop/300/190/2330258.jpg)