동아ST·알테오젠·삼천당제약 등 제약바이오 기업도 ‘참전’
셀트리온과 삼성바이오에피스가 국내 바이오시밀러 산업을 주도하는 가운데 틈새를 공략하는 중소 바이오시밀러 기업들이 존재감을 키우고 있다. 프레스티지바이오파마, 에이프로젠 등은 생산 인프라 구축과 상용화 과정에서 가시적인 성과를 내고 있다.
3일 제약‧바이오업계에 따르면 국내 바이오시밀러 시장은 셀트리온과 삼성바이오에피스 중심의 양강 체제가 구축된 것으로 평가된다. 두 기업은 각각 미국과 유럽 등 선진국에서 수조 원대 매출을 올리며 글로버 시장 공략에서 성과를 내고 있다. 이러한 구도 속에서도 중소 제약바이오기업들이 시장의 빈틈을 공략하며 영역을 확장하고 있다.
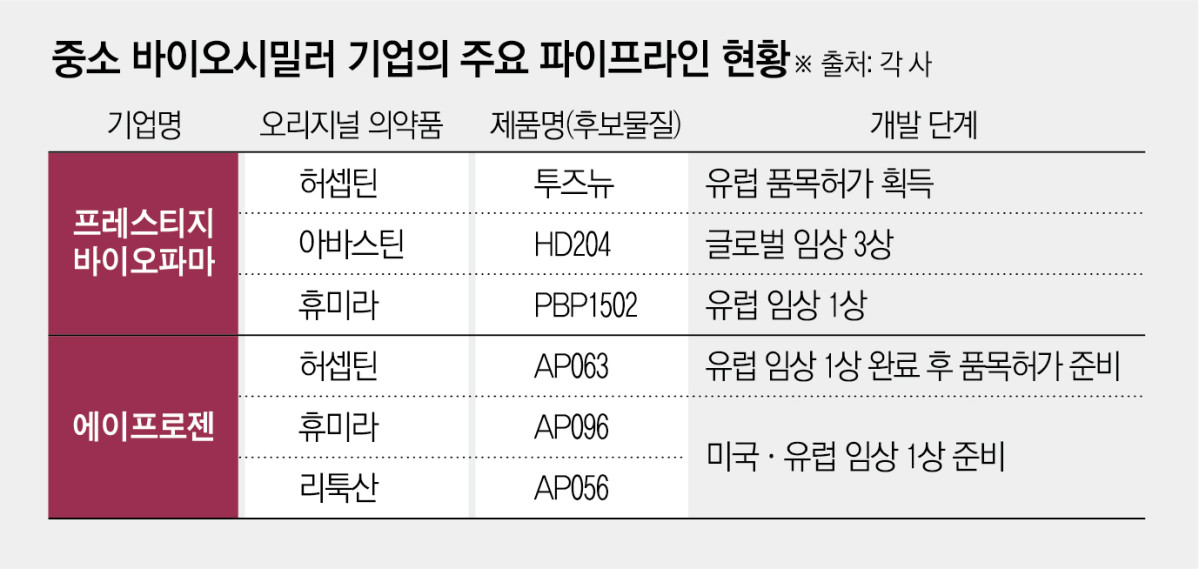
프레스티지바이오파마는 지난해 9월 유럽에서 허셉틴의 바이오시밀러 ‘투즈뉴’의 허가를 받았다. 셀트리온, 삼성바이오에피스에 이어 국내 기업으로는 세 번째다. 올해 5월에는 글로벌 제약사 테바와 유럽 30여개 국에 대한 라이선스 및 공급계약을 맺으며 출시를 앞두고 있다. 이외 아바스틴 바이오시밀러 ‘HD204’는 글로벌 임상 3상, 휴미라 바이오시밀러 ‘PBP1502’는 유럽에서 임상 1상 중이다.
에이프로젠은 유럽에서 허셉틴 바이오시밀러 ‘AP063’ 임상 1상을 완료하고 3상 없이 품목허가를 추진 중이고, 휴미라 바이오시밀러 ‘AP096’과 리툭산 바이오시밀러 ‘AP056’은 미국과 유럽에서 임상 1상을 준비 중이다. 일본에서는 이미 레미케이드 바이오시밀러를 판매 중이다.
바이오시밀러 전문 기업은 아니지만, 일부 제약사와 바이오 기업도 이 시장에 뛰어들고 있다. LG화학은 엔브렐 바이오시밀러 ‘유셉트’와 휴미라 바이오시밀러 ‘젤렌카’, 종근당은 네스프 바이오시밀러 ‘네스벨’과 루센티스 바이오시밀러 ‘루센비에스주’를 개발해 판매 중이다. 동아ST는 지난해 미국과 유럽에서 자가면역질환 치료제 스텔라라 바이오시밀러 ‘이뮬도사’의 품목허가를 받고 유럽에 출시했다.
알테오젠은 자회사 알테오젠바이오로직스를 통해 유럽에서 황반변성 치료제 아일리아 바이오시밀러 ‘아이럭스비’의 품목허가 권고 의견을 받아 승인을 앞두고 있고, 삼천당제약은 캐나다에서 아일리아 바이오시밀러 ‘SCD411’의 품목허가를 획득했다.
기업들이 바이오시밀러 시장에 진출하는 이유는 신약 대비 개발 기간이 짧고 개발・허가 성공률이 높아서다. 고가 바이오의약품의 특허 만료와 의료비 절감 수요가 맞물리며 시장 규모는 계속 확대되고 있다. 실제로 글로벌 바이오시밀러 시장은 매년 꾸준히 성장해 2033년에는 200조 원 규모에 이를 것으로 전망된다. 기존에 셀트리온과 삼성바이오에피스가 주도했던 구도에서 ‘제3의 주자’들이 등장해야 한다는 목소리도 나온다.
바이오 업계 한 관계자는 “셀트리온과 삼성 같은 대형사와 차별화된 전략을 갖춘 중소기업이 공존해야 한국 바이오시밀러 산업도 지속가능한 생태계를 구축할 수 있다”며 “정부의 지원과 민간의 전략 투자가 맞물려야 진정한 글로벌 경쟁력이 강화될 것”이라고 말했다.
다만 중소기업에게 국내 시장은 여전히 녹록지 않다. 특허청과 한국특허기술진흥원이 최근 발표한 보고서에 따르면, 낮은 특허 장벽에도 불구하고 바이오시밀러의 국내 점유율은 여전히 미미한 수준이다. 실제로 애브비의 휴미라는 국내 시장에서 90% 이상, 존슨앤드존슨의 레미케이드는 60% 이상의 점유율을 유지하고 있다. 대기업도 점유율 확보에 고전하는 상황에서 중소기업에게는 더 높은 진입 장벽이 존재한다.
보고서는 이러한 차이를 단순한 특허 문제가 아닌 제도와 시장 구조, 의료진과 환자의 인식 등 복합적인 요인에서 비롯된 것으로 분석했다. 국내는 오리지널 의약품과 바이오시밀러 간 가격 차이가 10~15%에 불과하고, 환자 부담금 차이도 거의 없다. 또 의료진은 효능과 안전성에 대한 불신으로 처방을 꺼리며 환자 역시 오리지널에 대한 심리적 신뢰가 높다. 따라서 바이오시밀러 처방 인센티브 제공, 환자 인식 개선 등 제도적 보완과 인식 전환이 필요하다는 의견이다.

![[단독] ‘삼바 재감리’서 감리위 패싱한 금융당국⋯“정당성 없다” 퇴짜 [흔들리는 금융감독 방정식]](https://img.etoday.co.kr/crop/140/88/1265555.jpg)
![미국·이란 교착 상태에도 뉴욕증시 S&P500·나스닥 또 최고치 [종합]](https://img.etoday.co.kr/crop/140/88/2327001.jpg)

![균형발전 역행하는 하늘길 ‘쏠림’…공항 경쟁력 다시 점검해야 [국민 위한 하늘길 다시 짜자①]](https://img.etoday.co.kr/crop/140/88/2326834.jpg)

![[단독] 한컴, '권고사직 통보 후 재배치' 이례적 인사 진통...고용 불안 혼란](https://img.etoday.co.kr/crop/140/88/2157212.jpg)




![전기차 로봇 다 하는데 어이 없게 저평가된 '이 주식' ㅣ 염승환 LS증권 이사 [찐코노미]](https://i.ytimg.com/vi/Y459xW8xD80/mqdefault.jpg)


![[컨콜] HD현대일렉트릭 "그룹사 차원 육상발전협의체 가동"](https://img.etoday.co.kr/crop/85/60/2292542.jpg)







![망 사용료 다시 꺼낸 美…계산서는 누구에게 [이슈크래커]](https://img.etoday.co.kr/crop/300/170/2327331.jpg)
![국회 본회의, 공직선거법 일부개정법률안 '가결' [포토]](https://img.etoday.co.kr/crop/300/190/2327390.jpg)