국내 기업들의 기술력으로 탄생한 수두백신이 글로벌 무대에서 빠르게 입지를 넓히고 있다. 10년 내 8조 원 규모로 불어날 것으로 예상되는 수두백신 시장에서 우리 기업들이 활약하면서 K백신의 경쟁력을 확인하는 것은 물론 공급망 다변화에도 기여하고 있다는 평가다.
28일 업계에 따르면 GC녹십자는 태국과 베트남에서 수두백신 ‘배리셀라주’의 2회 접종(2도즈) 임상 3상을 추진한다. 국내 제약사가 수두백신 2회 접종 임상에 진입하는 첫 사례다.
수두백신 2회 접종은 미국과 캐나다, 일본, 유럽 등 전 세계 28개국에서 권고하면서 표준으로 자리잡고 있다. 1회 접종 후 발생 가능한 돌파 감염의 위험을 막기 위해서다. GC녹십자는 2027년 하반기까지 임상을 마무리하고, 동남아시아 국가를 중심으로 품목허가에 나설 계획이다.
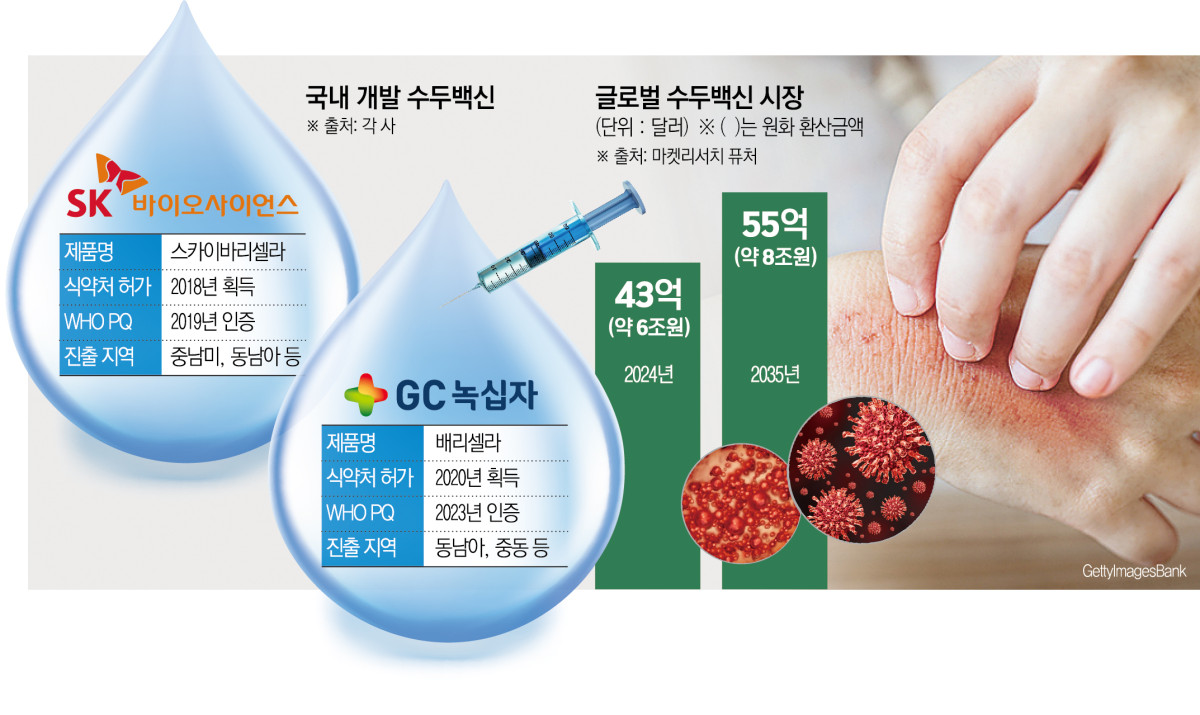
배리셀라주는 GC녹십자가 자체 개발한 ‘MAV/06’ 균주를 사용한 생백신이다. 높은 바이러스 함량과 고수율이 특징이며, 전 세계 최초로 무균 공정 시스템을 통해 항생제 없이 생산한다. 2020년 식품의약품안전처 허가를 받았으며, 2023년에는 세계보건기구(WHO) 사전적격성평가(PQ) 인증을 획득했다. WHO PQ 인증은 유니세프와 범미보건기구(PAHO) 등 국제연합(UN) 산하기관이 주관하는 입찰에 참여하기 위한 필수 자격이다.
GC녹십자는 지난달 베트남에서 배리셀라주의 품목허가를 받는 등 국가별 인허가에 속도를 내고 있다. 개별 시장 진출과 국제 조달 기구 입찰을 병행해 글로벌 입지를 강화하는 전략이다.
회사 관계자는 “연내 사우디아라비아 허가를 기대하고 있다. 동남아와 중동을 중심으로 시장을 넓히는 한편, PAHO 입찰도 참여한 상태”라고 설명했다.
글로벌 영향력이 커지면서 배리셀라의 매출 기여도도 점차 높아질 것으로 기대된다. GC녹십자는 연평균 30%씩 몸집을 불려 2028년까지 700억 원 이상의 매출을 달성하는 것이 목표다.
함께 경쟁을 벌이는 백신은 SK바이오사이언스의 ‘스카이바리셀라주’다. 2018년 식약처 허가를 받고, 이듬해에는 글로벌 제약사의 제품에 이어 세계 2번째로 WHO PQ 인증까지 확보했다.
SK바이오사이언스는 2022년 PAHO 입찰에서 첫 수주에 성공한 이후 중남미 지역에 꾸준히 스카이바리셀라주를 공급하고 있다. 올해 2월에는 PAHO로부터 2027년까지 공급해 줄 것을 사전 통지받아 6년 연속 공급을 확정지었다.
중남미에 성공적으로 자리 잡은 SK바이오사이언스는 태국과 말레이시아, 튀르키예, 파키스탄, 칠레, 멕시코 등 10여 개국의 허가도 획득, 시장 확대에 박차를 가하고 있다.
개발도상국의 수두 유병률 증가와 함께 백신 접종의 중요성에 대한 인식이 높아지면서 수두백신 시장은 꾸준히 성장할 전망이다. 글로벌 시장조사기관 마켓리서치퓨처에 따르면 2024년 43억 달러(약 6조 원) 규모로 추산된 이 시장은 2035년 55억 달러(약 8조 원)에 이를 것으로 예상된다.







![[단독] 대이란 금융제재 명분 흔들렸다…한은, 멜라트 예치 거부 소송서 패소](https://img.etoday.co.kr/crop/140/88/2339839.jpg)






![갑상선암 방심 금물…공격적인 유형 주의해야 [e건강~쏙]](https://img.etoday.co.kr/crop/85/60/2339877.jpg)








![Vol. 7 초고가 펫 케어: 슈퍼리치들의 반려동물이 사는 세상 [THE RARE]](https://img.etoday.co.kr/crop/300/170/2339687.jpg)
!['초록색 세이렌 로고를 향한 달라진 시선' [한컷]](https://img.etoday.co.kr/crop/300/190/2339918.jpg)