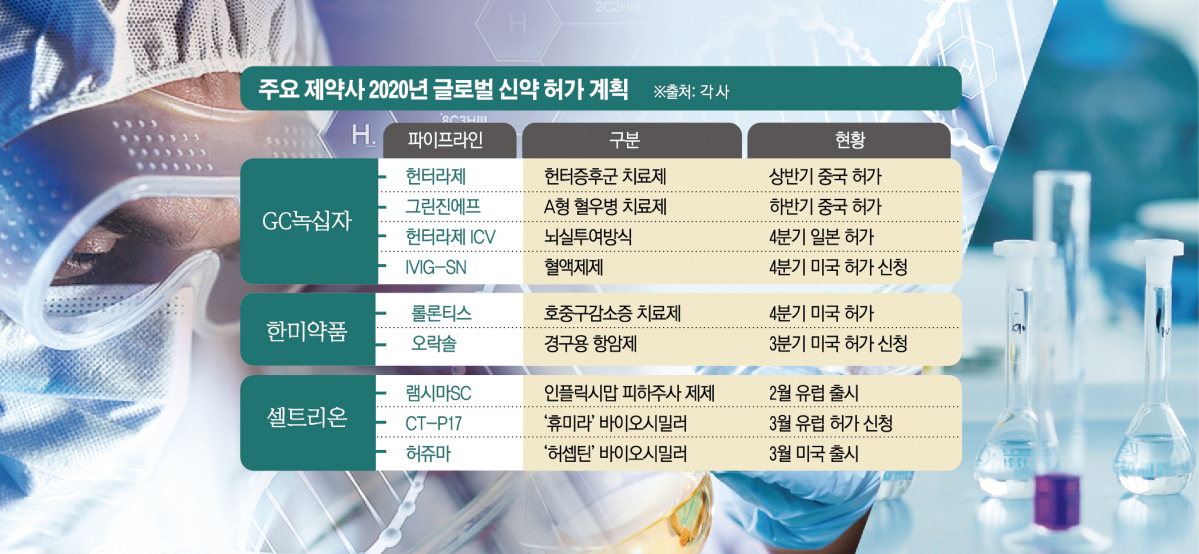
헌터라제는 GC녹십자가 세계 두 번째로 개발한 헌터증후군 치료제다. 헌터증후군은 IDS(Iduronate-2-sulfatase) 효소 결핍으로 골격 이상, 지능 저하 등을 가져오는 선천성 희귀질환이다. 남아 15만 명 가운데 1명꼴로 발생한다.
중국 내 헌터증후군 환자는 유병률 기준 3000명 정도로 예상된다. 헌터라제는 지난해 국내에서만 약 180억 원의 매출을 올렸다. 국내 환자 규모가 80명가량에 불과한 점을 고려하면, 중국은 거대한 잠재력을 가진 시장이다.
중국은 아직 헌터증후군 치료제로 허가받은 의약품이 없다. 헌터라제가 허가를 받으면 샤이어가 개발한 '엘라프라제'를 제치고 시장을 선점할 수 있다. 중국 국가약품감독관리국(NMPA)은 헌터라제를 우선 심사대상으로 지정, 상반기 중 허가가 유력하다.
GC녹십자 관계자는 "중국은 아직 헌터증후군 치료제 시장이 형성되지 않아 허가 직후 실적에 반영되지는 않겠지만, 환자 수가 월등히 많은 만큼 점진적인 성장세를 예상한다"고 설명했다.
헌터라제에 이어 하반기에는 그린진에프가 대기하고 있다. 그린진에프는 3세대 유전자재조합 방식의 A형 혈우병 치료제다. 중국의 혈우병 치료제 시장은 최근 유전자재조합 제제 중심으로 재편되고 있어 경쟁 제품 사이에서도 수익성을 확보할 수 있을 것으로 예상된다.
GC녹십자는 중국 외에도 일본에서 뇌실 투여 방식인 '헌터라제 ICV'의 품목허가를 올해 3월 신청했다. 헌터라제 ICV는 일본 후생노동성으로부터 희귀의약품에 지정되면서 허가 기간이 단축돼 연말께 승인이 가능하다.
이와 함께 회사는 혈액제제 'IVIG-SN' 10% 제품으로 세계 최대 의약품 시장 미국의 문을 두드린다. 올 4분기 미국 식품의약국(FDA)에 신약허가신청(BLA)를 제출할 계획이다. 목표대로 2021년 승인을 받으면 이듬해 5% 제품의 허가에도 도전할 계획이다.

롤론티스는 한미약품의 독자 개발 플랫폼 기술 랩스커버리가 적용된 지속형 주사제다. 랩스커버리는 단백질 의약품의 반감기를 늘려 약효를 지속시키고 투약 편의성을 높이는 기술력이다.
스펙트럼은 지난해 10월 FDA에 시판허가를 위한 보완자료를 제출, FDA는 12월 본격적인 심사에 들어갔다. 올해 10월까지 FDA의 검토를 거쳐 4분기 중 결과를 확인할 수 있다.
미국의 호중구감소증 치료제 시장은 4조 원 규모에 달한다. 현재 암젠의 '뉴라스타'가 이 시장을 독점하고 있다. 롤론티스가 허가를 받으면 15년 만의 신약이 탄생한다. 롤론티스는 임상 3상을 통해 뉴라스타 대비 중증 호증구감소증 발현 기간의 비열등성 및 우수한 상대적 위험 감소율 등을 입증했다.
한미약품의 또 다른 파트너사 아테넥스는 경구용 항암신약 '오락솔'의 신약허가신청(NDA)를 추진하고 있다. 아테넥스는 FDA와 사전 미팅을 완료하고 3분기 NDA를 신청할 계획이다.
오락솔은 주사용 항암제를 경구용으로 전환하는 플랫폼 기술 '오라스커버리'가 적용된 혁신신약으로, 2011년 아테넥스에 기술수출됐다. 아테넥스는 오락솔의 임상 3상 시험에서 파클리탁셀 정맥주사 제형 대비 1차 유효성 평가 지표인 객관적 반응률(ORR)에서 유의성을 확인했다.

2월 독일에서 처음 처방된 램시마SC는 영국과 네덜란드 등 유럽 각국에 차례로 출시되고 있다. 셀트리온그룹의 해외 유통 및 마케팅을 담당하는 셀트리온헬스케어는 14개 법인 및 지점을 잇는 자체 직판망을 통해 램시마SC를 직접 판매한다. 연말까지 유럽 전체 TNF-α 억제제 시장의 90%에 해당하는 9조2000억 원 규모의 시장에 램시마SC를 선보일 예정이다.
셀트리온은 염증성장질환(IBD)을 포함한 전체 적응증에 대한 허가를 추가해 램시마SC를 키울 계획이다. 특히 셀트리온의 '직판' 프로젝트의 선봉장인 램시마SC를 통해 파트너사를 새어나가던 마진을 흡수, 수익성을 더욱 끌어올릴 것으로 보인다.
미국에는 유방암·위암 치료용 바이오시밀러 '허쥬마'까지 주력 바이오시밀러 3종을 모두 출시했다. 2016년 11월 '인플렉트라'로 미국에 첫발을 디딘 지 햇수로 4년 만이다. 이에 따라 총 16조 원 규모의 거대한 시장에서 점유율을 키워나가고 있다.
후속 바이오시밀러인 자가면역질환 치료제 'CT-P17'(성분명 아달리무맙)은 3월 유럽의약품청(EMA) 허가 신청을 완료했다. CT-P17의 오리지널 의약품은 애브비의 '휴미라'로, 지난해 글로벌 매출 약 23조 원을 기록한 블록버스터다. 셀트리온은 이미 다수의 휴미라 바이오시밀러가 포진한 경쟁 상황을 고농도 제형으로 타개할 방침이다.
셀트리온 관계자는 "2030년까지 신규 제품을 매년 하나씩 선보이겠다는 목표가 차질없이 진행 중"이라며 "글로벌 대형 제약사로 성장하기 위해 다양한 포트폴리오를 확보해야 한다"고 말했다.



![[종합] 삼성전자 ‘역대 최대’…반도체 53조, 2분기도 HBM 질주](https://img.etoday.co.kr/crop/140/88/2328495.jpg)

![연준, 금리 동결로 파월 시대 마무리…반대 4표로 내부 분열 부각[종합]](https://img.etoday.co.kr/crop/140/88/2328317.jpg)


















![현대차는 재평가, 기아는 저평가...투자 포인트는 [찐코노미]](https://img.etoday.co.kr/crop/300/170/2328645.jpg)
!['컴백홈' 5년 만에 돌아왔다, 서울사진축제...6월 14일까지 [포토]](https://img.etoday.co.kr/crop/300/190/2328556.jpg)