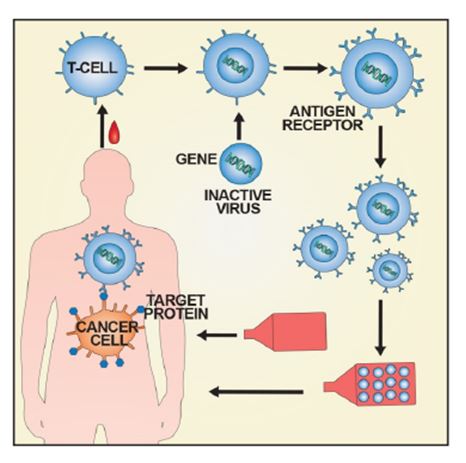
한국노바티스의 키메라 항원 수용체 T세포(CAR-T) 치료제가 국내 1호 첨단바이오의약품으로 허가받았다.
식품의약품안전처는 한국노바티스가 허가 신청한 세계 최초 키메라 항원 수용체 T세포(CAR-T) 치료제 ‘킴리아주(티사젠렉류셀)’를 첨단재생바이오법에 따른 제1호 첨단바이오의약품으로 허가했다고 5일 밝혔다.
첨단바이오의약품은 세포치료제·유전자치료제 등 살아있는 세포·조직이나 유전물질 등을 원료로 한 의약품을 뜻한다. ‘키메라 항원 수용체 T세포’는 면역세포(T세포)의 수용체 부위와 암 세포 표면의 특징적인 항원 인식 부위를 융합한 유전자를 환자의 T세포에 도입한 것으로, 암세포의 표면 항원을 특이적으로 인지해 공격하는 기능을 갖는다.
‘킴리아주’는 환자에게 채취한 면역세포(T세포) 표면에 암세포의 특정 항원을 인지할 수 있도록 유전정보를 도입한 후 환자의 몸에 주입하는 방식의 항암제다. 이 약은 다른 치료제를 선택하는 것이 제한적인 재발성·불응성 혈액암 환자에게 한 번의 투여로 명백히 개선된 유익성을 보인 혁신적 면역세포 항암제로, 미국에서는 획기적 의약품, 유럽에서는 우선순위의약품(PRIME)으로 각각 지정된 후 허가받았다.
식약처는 “첨단재생바이오법의 심사기준에 따라 신청 의약품에 대한 품질, 안전성·효과성, 시판 후 안전관리계획 등에 대해 과학적으로 철저하게 심사·평가했고, 혈액암 분야 의료현장 전문가 등이 포함된 중앙약사심의위원회에서 해당 제품의 허가 타당성과 제도 부합성에 대한 자문을 거쳤다”라고 밝혔다.
이 약은 첨단재생바이오법에 따른 ‘장기추적조사’ 대상 의약품으로, 이상사례 현황에 대해 투여일로부터 15년간 장기추적해야 하고, 최초 판매한 날부터 1년마다 장기추적 조사한 내용과 결과 등을 식약처에 보고해야 한다.

![한타바이러스 등장…뜻·증상·백신·치사율 총정리 [이슈크래커]](https://img.etoday.co.kr/crop/140/88/2330748.jpg)
![수학여행 가는 학교, 2곳 중 1곳뿐 [데이터클립]](https://img.etoday.co.kr/crop/140/88/2330760.jpg)
!["대학 축제 라인업 대박"⋯섭외 경쟁에 몸살 앓는 캠퍼스 [이슈크래커]](https://img.etoday.co.kr/crop/140/88/2330763.jpg)
![삼성전자 파업의 역설…복수노조 시대 커지는 ‘노노 갈등 비용’ [번지는 노노 갈등]](https://img.etoday.co.kr/crop/140/88/2330599.jpg)
![[단독] 나프타값 내리는데…석화사 5월 PP값 또 인상 통보](https://img.etoday.co.kr/crop/140/88/2329959.jpg)
![코스피 6000→7000까지 70일⋯‘칠천피’ 이끈 5대 고수익 섹터는?[7000피 시대 개장]](https://img.etoday.co.kr/crop/140/88/2330299.jpg)















![“골프웨어 넘어 라이프스타일로 확장”...북촌에 둥지 튼 63평 ‘말본가옥’[가보니]](https://img.etoday.co.kr/crop/85/60/2330608.jpg)
!["대학 축제 라인업 대박"⋯섭외 경쟁에 몸살 앓는 캠퍼스 [이슈크래커]](https://img.etoday.co.kr/crop/300/170/2330763.jpg)
!['184m' 기네스북 오른 청라하늘대교 전망대 개장 [포토로그]](https://img.etoday.co.kr/crop/300/190/2330807.jpg)