뉴지랩파마 신약개발 전문 자회사 ‘뉴지랩테라퓨틱스’는 비소세포성 폐암 치료제 탈레트렉티닙의 임상 2상 유효성 중간평가에서 1차 치료군 환자 3명 전원에게서 부분 관해가 확인됐다고 25일 밝혔다.
더불어 2차 치료군 대상 임상시험에서도 환자 6명 중 3명에게서 부분 관해가 관찰됐다고 한다.
부분 관해는 치료 후 암 병변 크기가 30% 이상 감소해 환자의 상태가 뚜렷이 개선되고 있는 상황으로, 환자 상태 개선을 뜻한다.
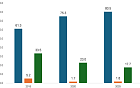
이번 중간평가는 글로벌 제약사 ‘안허트테라퓨틱스’가 지난해 미국 ASCO(미국임상암학회)에서 발표한 텔레트렉티닙의 글로벌 임상 2상 중간결과를 웃도는 결과를 냈다. 인허트테라퓨틱스 발표에 따르면 탈렉트렉티닙은 1차 치료군에서 92.5%, 2차 치료군에서 50%의 객관적 반응률(ORR)을 보였다.
비소세포성 폐암 ROS-1 변이 표준 치료제인 화이자 ‘젤코리’는 승인 당시 1차 치료군에서 ORR 73%, 로슈 ‘로즐리트렉’은 78%를 나타내 이를 웃도는 결과를 낸 탈레트렙티닙은 향후 환자에게 좋은 치료 옵션이 될 것이라는 게 회사 측 설명이다.
뉴지랩테라퓨틱스는 안허트테라퓨틱스와 함께 한국·미국·일본에서 동시에 탈레트렉티닙 글로벌 임상 2상을 진행 중이다. 국내에서는 10명의 환자를 모집했다. 임상시험이 진행 중인 9명의 환자 중 6명에게서 부분 관해가 확인됐다.
뉴지랩파마 관계자는 “올해 상반기 내 임상 2상을 종료하고 신속심사 지정을 거쳐 식약처에 신약품목허가(NDA) 신청을 할 계획”이라며 “지난해 미국 FDA로부터 혁신치료제(BTD) 지정을 받아 임상이 끝나는 대로 조건부 사용승인이 가능해 빠른 상업화도 기대할 수 있다"고 말했다.
한편, 이번 1차 치료군 중간결과는 서울 아산병원, 고려대학교 구로 병원, 부산대 병원에서 진행된 임상시험의 중가결과로, 그 외 화순 전남대병원과 부산대 양산병원에서 진행된 임상시험 진행결과도 조만간 발표될 예정이다.

![한타바이러스 등장…뜻·증상·백신·치사율 총정리 [이슈크래커]](https://img.etoday.co.kr/crop/140/88/2330748.jpg)
![수학여행 가는 학교, 2곳 중 1곳뿐 [데이터클립]](https://img.etoday.co.kr/crop/140/88/2330760.jpg)
!["대학 축제 라인업 대박"⋯섭외 경쟁에 몸살 앓는 캠퍼스 [이슈크래커]](https://img.etoday.co.kr/crop/140/88/2330763.jpg)
![삼성전자 파업의 역설…복수노조 시대 커지는 ‘노노 갈등 비용’ [번지는 노노 갈등]](https://img.etoday.co.kr/crop/140/88/2330599.jpg)
![[단독] 나프타값 내리는데…석화사 5월 PP값 또 인상 통보](https://img.etoday.co.kr/crop/140/88/2329959.jpg)
![코스피 6000→7000까지 70일⋯‘칠천피’ 이끈 5대 고수익 섹터는?[7000피 시대 개장]](https://img.etoday.co.kr/crop/140/88/2330299.jpg)








![코스피, 역대급 상승에 3일만에 거래대금 150조 넘어…대형주 거래 쏠림은 심화 [7000피의 역설]](https://img.etoday.co.kr/crop/85/60/2330814.jpg)
![[채권마감] 종전 기대감…통안·국고채 4거래일만 전구간 강세](https://img.etoday.co.kr/crop/85/60/2330367.jpg)
![[오늘의 주요공시] 카카오·SK바이오팜·HD현대중공업 등](https://img.etoday.co.kr/crop/85/60/2330316.jpg)
![[급등락주 짚어보기] 종전 기대·AI 광통신 확산…태영건설우·빛샘전자 등 '上'](https://img.etoday.co.kr/crop/85/60/2330799.jpg)
![[장외시황] 아이벡스메디칼시스템즈, 코스닥 상장예비심사 청구](https://img.etoday.co.kr/crop/85/60/2330787.jpg)

![[환율마감] 외인 코스피 사상최대 순매도…원·달러 1440원대 찍고 되돌림](https://img.etoday.co.kr/crop/85/60/2317033.jpg)

!["대학 축제 라인업 대박"⋯섭외 경쟁에 몸살 앓는 캠퍼스 [이슈크래커]](https://img.etoday.co.kr/crop/300/170/2330763.jpg)
!['184m' 기네스북 오른 청라하늘대교 전망대 개장 [포토로그]](https://img.etoday.co.kr/crop/300/190/2330807.jpg)