셀리버리는 개발 중인 코로나19 면역치료제 iCP-NI의 글로벌 임상 2상 적응증으로 중증 패혈증을 추가한다고 5일 밝혔다.
iCP-NI는 개발 초기 중증 염증이 촉발돼 환자를 죽음에 이르게 하는 패혈증 치료를 목적으로 임상개발을 시작했으나, 2020년 초 코로나19 바이러스 감염으로 인한 염증 및 폐 손상으로 코로나19 감염병의 중증, 위중증 및 사망하는 환자들을 위한 임상개발에 집중해 왔다.
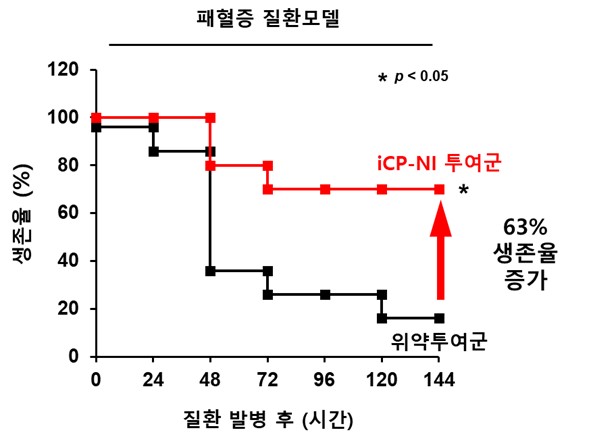
셀리버리 임상개발 책임자는 “현재 미국 및 유럽에서 임상 1상을 기다리고 있고, 임상 2상부터는 코로나19와 패혈증, 신종 인플루엔자 등 감염성 질환들에 대한 여러 건의 임상시험이 진행된다”면서 “패혈증 관련해서는 세균 감염 및 중증 염증으로 7일 내 사망하는 질환모델의 생존율이 63% 증가하는 치료 효능이 있었다”고 설명했다.
셀리버리는 패혈증에 대한 치료효능 입증을 비롯해 임상에 적용할 수 있는 수준의 투약 프로토콜 설정까지 마쳤다. 위탁시험기관을 통해 동일한 패혈증 질환모델을 대상으로 임상프로토콜에 따라 iCP-NI를 투여하는 재현성 검증시험을 진행했을 때도 동일한 수준의 생존율 증가 효능을 입증했다. 미국과 유럽의 임상규제기관에 제출할 모든 효능평가시험의 결과보고서와 국제공통기술문서의 확보도 마쳤다.
회사 관계자는 “이미 코로나19 임상개발을 위한 안전성평가 및 제형개발, 물질안정성평가가 완전히 끝나 임상 1상 후 코로나19 감염병과 패혈증을 대상으로 한 임상 2상 시험이 동시에 진행될 것”이라며 “유럽의약품청(EMA)와 미국 식품의약국(FDA)의 10월 초 임상 승인을 기다리고 있으며, 임상시험을 위한 병상확보 등의 사전작업 등은 모두 완료된 상태”라고 말했다.

![[단독] HD현대·한화 이어 삼성까지⋯美 함정 'MRO' 전격 참전 [K-정비 벨트 확장]](https://img.etoday.co.kr/crop/140/88/2328229.jpg)

![연준, 금리 동결로 파월 시대 마무리…반대 4표로 내부 분열 부각[종합]](https://img.etoday.co.kr/crop/140/88/2328317.jpg)


![흐린 날씨 속 ‘건조 주의’...일교차 15도 안팎 [날씨]](https://img.etoday.co.kr/crop/140/88/2328193.jpg)
![선거앞 달콤한 유혹…돈풀기 경쟁에 내몰린 교부세 [지자체 현금포퓰리즘]](https://img.etoday.co.kr/crop/140/88/2326643.jpg)













![[상보] 삼성전자 1분기 역대 최대 실적…영업익 반도체만 53조](https://img.etoday.co.kr/crop/85/60/2305629.jpg)


!["이런 건 처음 본다" 경악까지⋯'돌싱N모솔', 연프 판 흔들까 [엔터로그]](https://img.etoday.co.kr/crop/300/170/2328140.jpg)
!['황금 연휴' 중국-일본 관광객 20만명, 한국 찾는다 [포토]](https://img.etoday.co.kr/crop/300/190/2328095.jpg)