
만성신부전 관련 빈혈과 항암치료 후 빈혈 치료제로 쓰이는 2세대 EPO(Erythropoietin) 아라네스프/네스프(Aranesp/NESP)도 그 중 하나다. 전세계 시장 30억 달러(3조원) 이상으로 추정되는 네스프 바이오시밀러 개발에 국내에서는 종근당, 동아ST, CJ헬스케어 해외에서는 일본의 키세이 파마슈티컬스(Kissei pharmaceuticals)와 제이씨알 파마슈티컬스(JCR pharmaceuticals) 등이 뛰어들었다. 이들의 공략 대상은 우선 한국과 일본 시장으로 이를 발판으로 미국 시장(특허 2024년 이후에 만료)에 진출할 계획이다.
◇2세대 EPO 블록버스터 '네스프'
EPO는 골수에서 하루 2억개 정도의 적혈구 생산에 일조하는 생체유래물질이다. EPO는 골수에서 조혈모세포에 작용해 적혈구 원시세포의 분열과 분화를 자극해 빈혈(만성신부전 관련 빈혈, 항암치료 후 발생한 빈혈)을 치료한다. 암젠의 에포젠(Epogen)과 존슨앤드존슨의 프로크릿(Procrit)이 대표적으로 에포젠은 2017년 11억 달러, 프로크릿은 9억7000만 달러의 매출을 기록했다.
네스프는 암젠과 일본 쿄와하코기린이 공동 개발한 2세대 EPO다. 체내의 적혈구생성촉진인자(Erythropoietin)와 유사하게 명주쥐 난소유래세포주(CHO cell)에서 만들어낸 적혈구 생성 자극 단백질로 DNA 재조합기술에 의해 만들었다. 1세대 EPO가 1주일에 3회 투약하는 반면 네스프틑 1주일에 1번 또는 2주에 1번 투약하면 되도록 편의성을 개선했다.
2001년 6월 유럽 EMA에서 만성신부전 관련 빈혈과 항암치료 후 발생한 빈혈환자를 적응증으로 허가를 받았고, 그해 9월, FDA로부터 만성신부전과 관련된 빈혈 적응증으로 승인을 획득했다. 미국과 유럽, 캐나다, 동남아 등 전세계 40여 개국에서 판매되고 있다. 전세계 EPO 시장 규모는 2017년 기준 75억 달러, 그 중 네스프는 30억 달러에 이를 것으로 추정된다.
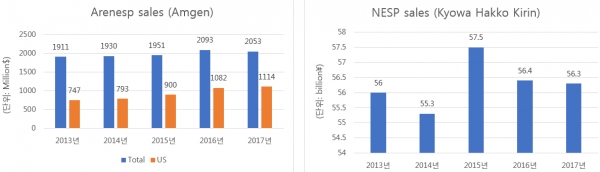
네스프는 암젠이 미국, 유럽, 호주 등에 쿄와하코기린이 일본, 한국, 싱가포르, 대만, 태국 등의 시장에 대한 판권을 보유하고 있다. 암젠의 실적을 살펴보면 2013년에는 19억1100만달러에서 2017년 20억5300만달러로 성장했다. 쿄와하코기린의 경우 2013년 560억엔에서 2017년 563억엔으로 성장세가 두드러지지는 않았다.
◇네스프의 메커니즘은? 1세대 EPO와의 차이점
우리 몸의 골수에서는 면역과 관련된 백혈구, 산소나 조직(tissue), 기관(organ)에서 발생한 노폐물을 운반하는 역할의 적혈구, 지혈에 중요한 혈소판과 같은 혈액세포를 생산한다. 하지만 이러한 골수의 조혈기능은 화학적 항암치료나 방사선 치료를 경험한 환자들에게서 현저하게 저하되는 경향을 보인다.
NESP는 체내 신장에서 생산되는 조혈기능 단백질인 적혈구생성촉진인자(Erythropoietin)와 유사하게 만들어낸 인공 조혈 단백질로 165개의 아미노산으로 이뤄졌다. 실제 인간 적혈구생성촉진인자가 3개의 올리고당 사슬을 가진 반면에, NESP는 5개의 N-올리고당 사슬을 가지고 있는데 2개의 추가적인 당사슬은 적혈구생성촉진인자 펩타이드 뼈대를 보완하는 역할을 하며, 이로 인해 분자량이 30000Da에서 37000Da까지 증가한다.
NESP는 적혈구생성촉진인자와 같은 메커니즘으로 적혈구생성을 자극한다. 적혈구생성촉진인자는 신장에서 만들어지고 저산소증에 대한 반응으로 혈류에 배포된다. 저산소 상태가 되면 적혈구생성촉진인자는 혈류를 통해 골수로 이동해 전구줄기세포와의 상호작용을 통해 적혈구 생산을 증가시킨다.
만성신부전증 환자들은 내인성 적혈구생성촉진인자의 생산에 문제가 발생하게 되는데 이러한 결핍은 환자들이 겪는 빈혈의 첫번째 원인이다. NESP는 이러한 환자들에게 적용돼 적혈구 생성을 자극함으로써 빈혈을 치료한다.
성인 만성신부전환자에게 정맥주사 경로로 NESP를 적용했을 때 체액 농도-시간 분석결과, 분포 반감기 중간값은 대략 1.4시간이었고, 종결 반감기는 21시간으로 1세대 EPO와 비교했을 때 3배 이상의 반감기를 보였다. 만성신부전을 앓고 있는 12명의 소아환자에게 NESP를 적용했을 때 혈중농도와 반감기는 성인 만성 신부전 환자의 결과와 비슷한 양상으로 나타났다.
◇네스프 개발 경쟁 한국·일본 기업이 주도..종근당이 선두
네스프바이오시밀러 개발에는 국내 기업들이 발빠르게 도전하고 있다. 가장 앞선 것이 종근당의 ‘CKD-11101’로 국내에서 지난해 임상 3상을 완료했으며 현재 국내 발매를 위한 식약처 허가 심사 중에 있다. 일본의 후지제약공업에 기술을 수출했으며 일본에서도 임상을 진행하고 있다.
그 다음은 동아ST의 ‘DA-3880’다. 2014년 동아ST는 일본의 산와 가가쿠 SKK(Sanwa Kagaku Kenkyusho)에 기술을 수출했다. 2016년 9월 일본에서 상업화를 위한 임상3상을 진행하고 있으며 동아ST는 글로벌 임상3상을 진행하기 위해 준비하고 있다.
CJ헬스케어도 2017년 2월부터 국내 만성신부전증 환자 236명을 대상으로 NESP 바이오시밀러 ‘CJ-40001’의 임상 3상을 진행하고 있다. CJ는 2017년 9월 일본의 YL바이오로직스에 기술을 수출했으며 올해 2월에는 중국의 NCPC에 기술을 수출했다.
일본의 제약사들도 NESP 바이오시밀러 개발에 한창이다. 일본 진테크노사이언스(Gene techno science)는 ‘GBS-011’이라는 프로젝트명으로 2016년 9월부터 임상3상을 진행하고 있다. 또한 키세이 파마슈티컬스(Kissei pharmaceuticals)와 제이씨알 파마슈티컬스(JCR pharmaceuticals)가 공동개발 중인 ‘JR-131’은 올해 1월 오리지널 제품과 비교했을 때 동등한 효과를 나타내는 것을 확인하고 성공적으로 임상3상을 종료했다고 밝혔다.
네스프는 국내에서는 특허가 만료됐고(2015년) 일본에선 2019년, 미국에선 2024년까지 특허가 유지된다. 기업들은 한국과 일본에서 먼저 네스프 바이오시밀러를 출시해 시장성을 확인한 후 미국 시장에 진출하는 전략을 펼칠 것으로 예상된다. 미국 시장의 경우 1세대 EPO의 바이오시밀러가 이달 첫 허가(화이자 리타크릿)를 받을 정도로 진입 장벽이 높다.

![[알립니다] 2026 대한민국 금융대전 개최합니다](https://img.etoday.co.kr/crop/140/88/2342430.jpg)


![뉴욕증시, 트럼프 “이란 더 강하게 타격”에 하락...나스닥 1.98%↓ [종합]](https://img.etoday.co.kr/crop/140/88/2344542.jpg)

![美, 이란에 추가 공습…“여러 표적 대상 자위적 공습 개시” [상보]](https://img.etoday.co.kr/crop/140/88/2344537.jpg)
![월드컵 몸집 키운 FIFA…수입도 역대 최대 [북중미 월드컵 개막 ①]](https://img.etoday.co.kr/crop/140/88/2344404.jpg)











![[BioS]일동제약, 웰트와 ‘AI 디지털 융합의약품’ 개발 MOU](https://img.etoday.co.kr/crop/85/60/2344731.jpg)

!["인서울보다 준서울이 낫다"⋯동탄 끌어올린 건 '고소득 맞벌이' [집땅지성]](https://img.etoday.co.kr/crop/300/170/2344718.jpg)
![이상 기후-전쟁 여파로 수산물 물가 올라 [포토로그]](https://img.etoday.co.kr/crop/300/190/2344365.jpg)